研究室の紹介Laboratory
糖ペプチド合成
タンパク質の多くは糖鎖と結合した糖タンパク質として存在しています。このような糖タンパク質の機能や構造の解析には、その部分構造である糖ペプチド標品が必須であります。特に構造明解な糖ペプチド標品の量的供給には化学合成が用いられています。当研究室では糖ペプチドの合成に関する研究を行っておりますので、その紹介をいたします。
天然型糖鎖を有する糖ペプチドの合成
当研究室では化学-酵素法により、複雑な天然型糖鎖を有する糖ペプチドの合成法の開発に成功しました(J. Am. Chem. Soc誌1999年掲載)。
まず糖1残基を有する糖ペプチド(GlcNAc-ペプチド)を、チオエステル法と呼ばれる長鎖ペプチド合成技術を用いて化学合成しました。次に、天然物より調製した糖鎖アスパラギンを原料とし、この糖鎖部分を、毛カビの1種であるMucor hiemalis由来のedno–N-acetylglucosaminidase(EndoM)という酵素を用いて先ほど合成した「糖1残基を有する糖ペプチド」の糖部分に結合させ(この反応を糖鎖転移反応と言います)、複雑な天然型糖鎖を有する糖ペプチドを合成しました。
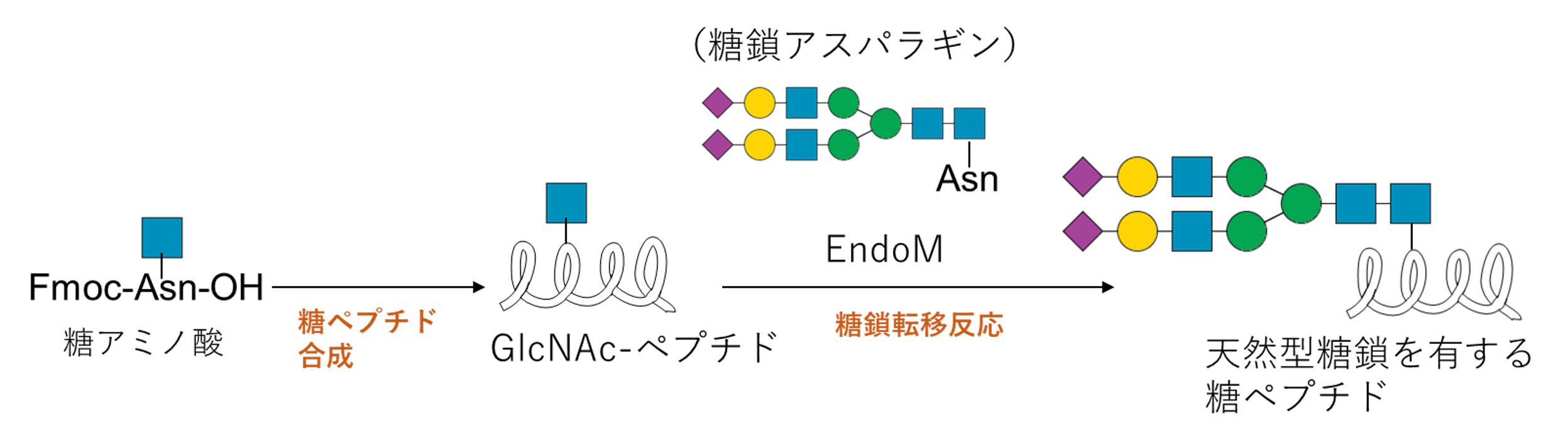
我々がこの研究成果を発表した当時(1999年)は糖鎖転移反応の収率はわずか9%程度でした(それでも当時は非常にインパクトのある結果でした)。しかし、その後世界中の多くの研究者たちによって糖鎖転移収率の向上が図られ、現在では収率が80%以上にまで向上し、様々な分野で汎用されている技術となっています。
関連論文
J. Am. Chem. Soc., 1999, 121, 284-290
“Synthesis of Glycopeptide Having Oligosaccharide : Chemoenzymatic Synthesis of Eel Calcitonin Analogs Having Natural N-Linked Oligosaccharides.”
Mamoru Mizuno, Katsuji Haneda, Reiko Iguchi, Ikuyo Muramoto, Toru Kawakami2, Saburo Aimoto, Kenji Yamamoto, and Toshiyuki Inazu
大阪大学、京都大学
酸性条件で除去できる糖ヒドロキシ保護基を使用した、簡便な糖ペプチド合成法の開発
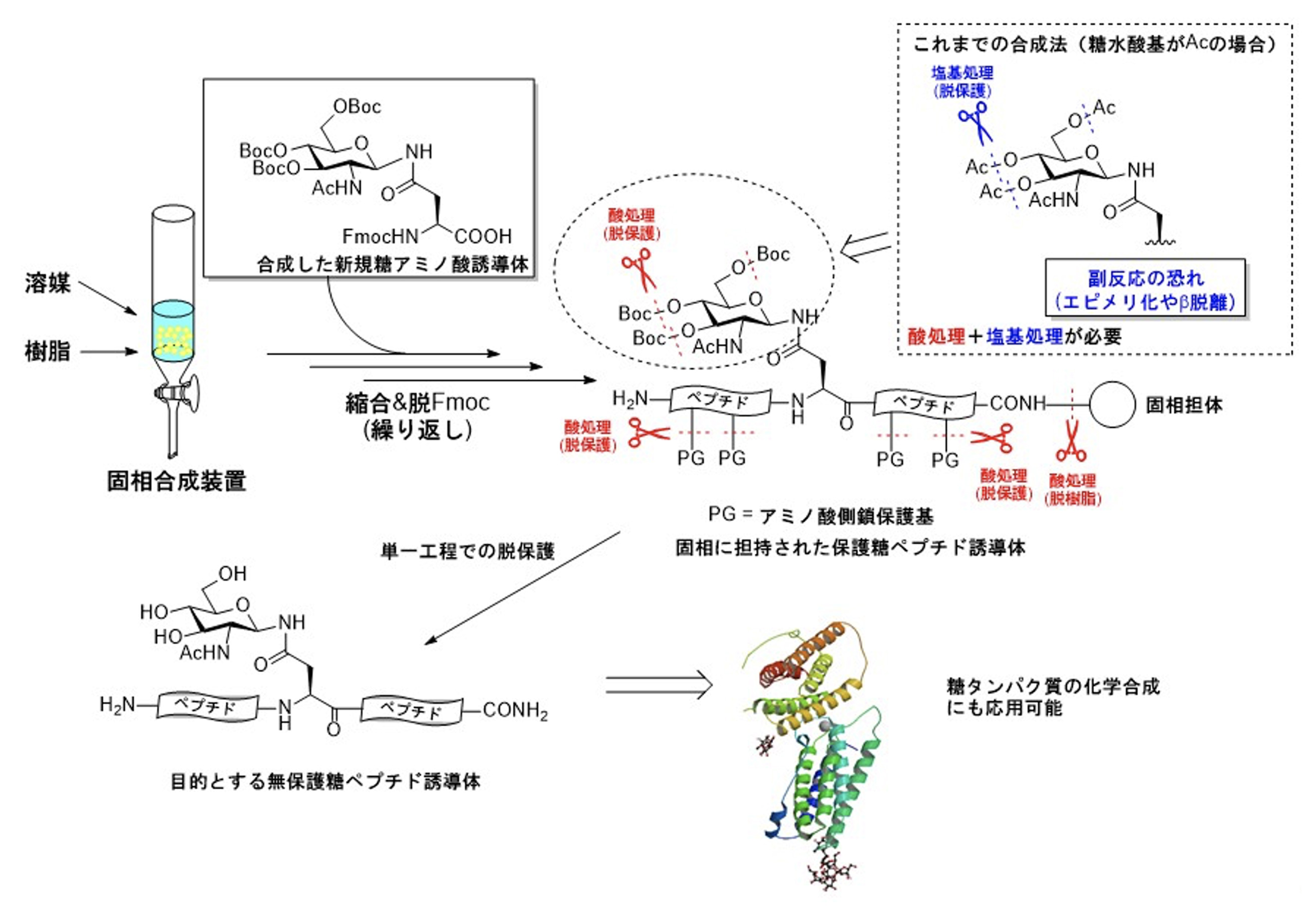
糖ペプチドの合成の際には、合成反応中の副反応(O-アシル化等)を防ぐために糖のヒドロキシ基を保護基で保護する必要があります。一般的にはアセチル基やベンジル基等が用いられていますが、これらはペプチド部位の脱保護反応条件では除去できないため、別途糖ヒドロキシ基保護基の除去が必要になります。さらに従来の糖ヒドロキシ基保護基の除去条件では副反応(糖鎖の分解や、ペプチド部位からの糖鎖の脱離等)が起こることが問題となっています。
このような糖ヒドロキシ基由来の副反応を回避するために、当研究室では糖ヒドロキシ基の保護基としてtert-butyloxycarbony(Boc)基を用いる手法を開発しました。本手法のポイントとしては、当研究室で開発した糖キドロキシ基をBoc基で保護した糖アミノ酸(O-Boc保護糖アミノ酸)を原料として使用することです。このBoc基はペプチド部位の保護基と一緒に除去できることから、従来の糖ペプチド合成で問題となっていた保護基由来の種々の副反応を抑制できる効率的な糖ペプチド合成法であります(Tetrahedron Lett.誌2019年掲載、特許第6605201号)。
関連論文
Tetrahedron Lett., 2019, 60, 151106 (https://doi.org/10.1016/j.tetlet.2019.151106)
“Efficient Synthesis of N- and O-linked Glycopeptides using Acid-Labile Boc Groups for the Protection of Carbohydrate Moieties”
Tomohiro Tanaka, Mika Shiraishi, Akio Matsuda and Mamoru Mizuno
